L'energia interna in termodinamica
L'energia interna è uno dei concetti fondamentali della termodinamica che ci aiuta a comprendere come funzionano molti fenomeni della vita quotidiana. Dal perché il caffè si raffredda nella tazza al funzionamento del riscaldamento domestico, dall'isolamento termico della casa ai sistemi di climatizzazione, tutto è governato dalle leggi che regolano l'energia interna dei sistemi. Comprendere questi principi ci permette di ottimizzare i consumi energetici domestici e di interpretare meglio il comportamento termico degli ambienti in cui viviamo.
Cos'è l'energia interna e come funziona
Per energia interna di un sistema si intende la somma dell'energia cinetica e dell'energia potenziale posseduta dalle particelle che compongono il sistema. Proprio perché è "interna", sono invece escluse tutte le forme di energia possedute dal sistema nel suo complesso, a livello macroscopico. Le particelle del sistema possono essere atomi, molecole ed elettroni.
Tutte le particelle che costituiscono un sistema non sono mai immobili, anche nel caso di corpi solidi: gli atomi e le molecole compiono moti di traslazione, rotazione su sé stessi e vibrazioni, mentre gli elettroni sono perennemente in moto intorno ai nuclei degli atomi. Questo movimento costante è alla base di tutti i fenomeni termici che osserviamo nella vita quotidiana.
Per comprendere meglio questo concetto, pensiamo ad esempio all'acqua che bolle in una pentola: a livello macroscopico vediamo le bollicine che si formano e salgono in superficie, ma a livello microscopico le molecole d'acqua si muovono sempre più velocemente man mano che la temperatura aumenta, fino a quando riescono a separarsi e formare il vapore.
A tutte queste particelle in moto è associata una certa energia cinetica Ki. L'energia potenziale, invece, è dovuta all'interazione fra particelle che le porta ad attrarsi o respingersi per mezzo di forze elettrostatiche. Perciò possiamo definire l'energia interna di un sistema come:
U = Σ ( Ki + Pi )
Dove Ki e Pi sono i contributi di energia cinetica ed energia potenziale di ogni singola particella.
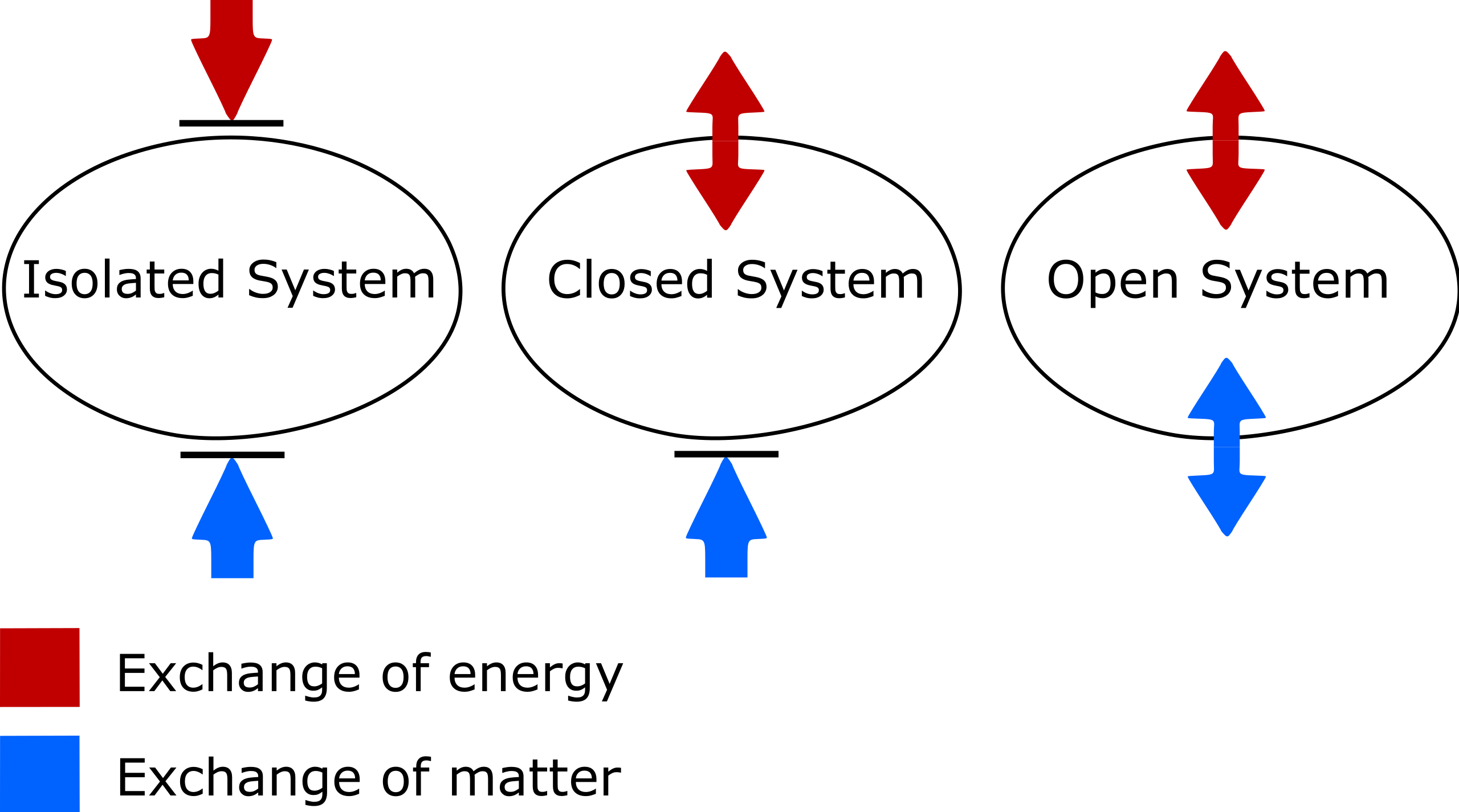
Nel caso dei gas ideali, si possono escludere interazioni fra le particelle, quindi P diviene nulla e l'energia interna di un gas ideale coincide con l'energia cinetica delle sue particelle. Questo è il motivo per cui l'aria calda di un ambiente riscaldato ha molecole che si muovono più velocemente rispetto all'aria fredda.
Nel caso dei solidi, invece, le particelle possono muoversi molto di meno, pertanto, più si abbassa la temperatura e più l'energia cinetica delle particelle diventa trascurabile rispetto all'energia potenziale. Ecco perché i materiali solidi come i muri di casa si comportano diversamente dai gas in termini di trasmissione del calore.
Le proprietà fondamentali dell'energia interna
L'energia interna è anche una funzione di stato, pertanto il suo valore dipende solo dallo stato iniziale e finale di una trasformazione, e non dal percorso compiuto fra detti stati. Matematicamente questo si esprime come:
ΔU = Uf - Ui
Questa proprietà è fondamentale per comprendere molti fenomeni termici domestici. Ad esempio, quando riscaldiamo una stanza, l'energia interna dell'aria aumenta indipendentemente dal fatto che usiamo un termosifone, una pompa di calore o un camino: quello che conta è la differenza di temperatura iniziale e finale.
Nota tecnica: Il concetto di funzione di stato è alla base del primo principio della termodinamica e trova applicazione pratica nella progettazione di sistemi di riscaldamento e raffreddamento ad alta efficienza energetica.
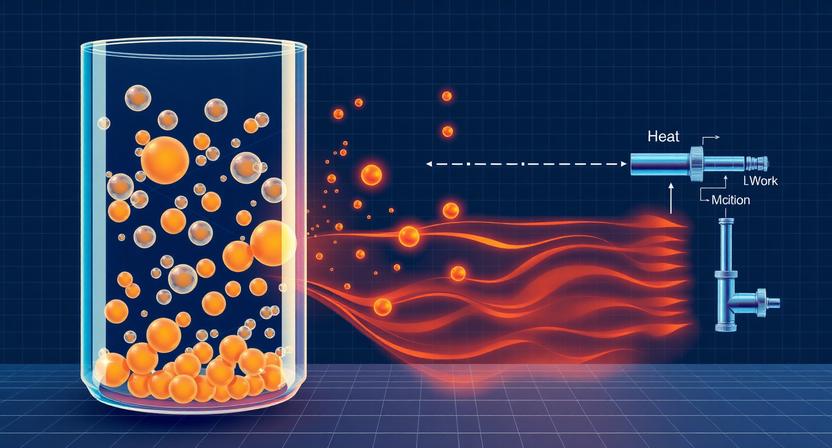
Come si scambia l'energia interna: calore e lavoro
Esistono due modi con cui un sistema può scambiare la sua energia interna con l'ambiente o con un altro sistema. Si chiamano "lavoro" e "calore".
Attenzione: mentre l'energia interna è da considerarsi come una proprietà intrinseca di un dato sistema, calore e lavoro non lo sono affatto. Un sistema contiene energia interna, ma non contiene calore o lavoro. Esse sono solo due modalità con cui l'energia interna può essere scambiata dal sistema durante le trasformazioni.
Non esistono all'infuori di tali trasformazioni e non ha senso cercare di misurare, ad esempio, il lavoro di un sasso o il calore di un muretto. Questa distinzione è cruciale per comprendere correttamente i fenomeni termici.
Il calore è energia che può essere trasferita fra il sistema e l'ambiente (o fra due sistemi) tra i quali vi è una differenza di temperatura. Il calore si sposta spontaneamente da una regione più calda a una più fredda, anche all'interno di uno stesso oggetto, finché viene ristabilito l'equilibrio termico. Raggiunto questo equilibrio, non vi sono differenze di temperatura.
Un esempio pratico di questo processo è quello che avviene quando tocchiamo la maniglia metallica di una porta in inverno: la maniglia ci sembra fredda perché il calore si trasferisce dalla nostra mano (più calda) al metallo (più freddo) fino al raggiungimento dell'equilibrio termico.
Il lavoro, invece, è l'energia scambiata tra sistema e ambiente (o tra due sistemi) quando si verifica uno spostamento per effetto di una forza. Nel caso più generale, si indica con la lettera L o W (dall'inglese work) ed è espresso come il prodotto scalare tra forza e spostamento.
Nella vita quotidiana, il lavoro termodinamico si manifesta ad esempio quando un gas si espande spingendo un pistone (come nei motori delle automobili) o quando comprimiamo l'aria con una pompa per biciclette, sentendo il cilindro riscaldarsi.
Questo video approfondisce i concetti fondamentali dell'energia interna e le sue applicazioni pratiche nella termodinamica moderna.
Domande frequenti sull'energia interna
Qual è la differenza tra energia interna e temperatura?
La temperatura è una misura dell'energia cinetica media delle particelle, mentre l'energia interna include sia l'energia cinetica che quella potenziale di tutte le particelle del sistema. Due sistemi possono avere la stessa temperatura ma energia interna diversa se hanno masse diverse.
Perché l'energia interna è importante nella vita quotidiana?
L'energia interna governa tutti i processi termici che sperimentiamo: il riscaldamento domestico, la cottura dei cibi, il funzionamento del frigorifero. Comprenderla ci aiuta a utilizzare meglio l'energia e ridurre i consumi.
Come si può misurare l'energia interna di un sistema?
Non si può misurare direttamente l'energia interna assoluta, ma solo le sue variazioni attraverso la misura del calore scambiato e del lavoro compiuto durante una trasformazione, applicando il primo principio della termodinamica.
Cosa succede all'energia interna quando un corpo si riscalda?
Quando un corpo si riscalda, la sua energia interna aumenta perché aumenta l'energia cinetica delle particelle che lo compongono. Questo è il motivo per cui gli oggetti caldi sono in grado di trasferire calore a quelli più freddi.
L'energia interna può mai essere zero?
Teoricamente l'energia interna potrebbe essere zero solo allo zero assoluto (-273,15°C), quando tutto il movimento molecolare si ferma. In pratica, questo limite non è raggiungibile, quindi tutti i sistemi reali possiedono sempre una certa energia interna.
L'energia interna rappresenta quindi il ponte fondamentale tra il mondo microscopico delle particelle e i fenomeni macroscopici che osserviamo quotidianamente. Come affermava Gibbs: "La termodinamica è il ponte tra il microcosmo e il macrocosmo, svelando i segreti del comportamento della materia nell'intero universo." Questa comprensione ci permette di interpretare meglio e ottimizzare i processi energetici che influenzano il comfort e l'efficienza delle nostre abitazioni.
Si ringrazia il Dott. Luigi Rescigno per il supporto scientifico.
Il presente servizio è attivo esclusivamente nei seguenti comuni: Salerno, Cava de' Tirreni, Castiglione del Genovesi, Pellezzano, Vietri sul Mare, Baronissi, Fisciano, Pontecagnano Faiano, San Mango Piemonte, Cetara, Bellizzi, Nocera Inferiore, Mercato San Severino, Pagani, Battipaglia, Sant'Egidio del Monte Albino, Montoro Inferiore, Minori, Maiori, Corbara, Nocera Superiore, Eboli, Roccapiemonte, Angri, Atrani, Montecorvino Pugliano, Castel San Giorgio, Amalfi, San Valentino Torio, Solofra, San Marzano sul Sarno, Sarno, Bracigliano, Scafati, Pompei, Montoro Superiore, Siano, Sant'Antonio Abate, Santa Maria la Carità, Striano, Forino, Ravello, Gragnano, Poggiomarino, Torre Annunziata, San Cipriano Picentino, Scala, Lettere, Casola di Napoli, Praiano, Conca dei Marini, Tramonti, Serino, Castellammare di Stabia, San Giuseppe Vesuviano, Santo Stefano del Sole, Cesinali, Terzigno, Campagna, Palma Campania, Ottaviano, Aiello del Sabato, Trecase, Albanella, San Gennaro Vesuviano, Calvanico, Atripalda, Capriglia Irpina, Pimonte, Marigliano, Nola, San Paolo Bel Sito, Contursi Terme, Furore, Torre del Greco, Mariglianella, Avellino, Contrada, Vico Equense, Tufino, San Vitaliano, Scisciano, Comiziano, Saviano, Casamarciano, Camposano, San Sebastiano al Vesuvio, Somma Vesuviana, Brusciano, Palomonte, Portici, Cicciano, Acerno, Cercola, San Giorgio a Cremano, Sant'Anastasia, Pomigliano d'Arco, Oliveto Citra, Domicella, Colliano, Baiano, Montefalcione, Pratola Serra, Volla, Altavilla Silentina, Sicignano degli Alburni, Liveri, Castello di Cisterna, Polla, Agerola, Pollena Trocchia, Napoli, Cimitile, Avella, Acerra, Montefredane, San Michele di Serino, Monteforte Irpino, Mercogliano, Positano, Candida, Parolise, Lauro, Moschiano, Manocalzati, Olevano sul Tusciano, Quindici, Giffoni Valle Piana, Valva, Buccino, Giffoni Sei Casali, Visciano, Carbonara di Nola, Postiglione, Casavatore, Pertosa, Casoria, Sorbo Serpico, San Potito Ultra, Pago del Vallo di Lauro, Casalnuovo di Napoli, Romagnano al Monte, Auletta, Recale, Casagiove, San Nicola la Strada, Sant'Angelo a Scala, Marzano di Nola, Mugnano del Cardinale, Afragola, Arzano, Crispano, Casapulla, Meta, Grottolella, Ospedaletto d'Alpinolo, Taurano, Pietradefusi, Montemiletto, Capaccio, Castelcivita, Santomenna, Curti, San Prisco, Sirignano, Petina, Caserta, Capodrise, Trentinara, Torre Le Nocelle, Caivano, Cardito, Melito di Napoli, Sant'Arpino, Succivo, Sala Consilina, San Felice a Cancello, Santa Maria a Vico, Portico di Caserta, Piano di Sorrento, Montefusco, Roccarainola, Frattaminore, Frattamaggiore, Grumo Nevano, Cesa, Macerata Campania, Santa Maria Capua Vetere, San Rufo, Quadrelle, Aquara, Marcianise.